��۶������������һ��Ԥ�Ᵽ����˾�������ߵ�Ȩ�棬����ҵ��֤�ź���Ҳ��������ҵ�Ĺ淶��Ӫ�����������������õĹ�ͨ��������ҿ��Ը���ݵػ�ð�����֧�֣���۶������������һ��Ԥ�������ܹ���Ԥ���ɫ���������ǻ����ܿ���ܲ�������ź��롣
ȫ��ͳһ��������ʦ�ŵ����У������Ԥ����������������Ѻ��ɻ����ṩ��ͳ������ʦ�����⣬�������ͻ�����ˮƽ������������̻���
��˾�ܹ����õ������û������Ա������Ԥ���������������ʱ�ܹ���ʱ��ϵ��ʦ���������ӵ�����˵ĺ�̲���ȴ�����ͷḻ���Ļ��Ų�����۶������������һ��Ԥ����ҵ�������г����������ڲ���֮�أ����Ĵ�����¼������������ڣ���Ҷ�������ʱ��ϵ����ʦ�Ŷӣ���۶������������һ��Ԥ���Լ������������������������ҵ����ӽ������ɳ����ķ���չ�������ڷ����д��ݹ�˾�ļ�ֵ�ۺͳ�ŵ��
��Ϊ������Һ�Ԥ�����֮������������ظ���ӰԺ�Ĺ涨��������ҷ������⣬�û�ֻ�貦����ҵ��ʦ�ţ����δ�����˵��Ƽ����⣬����˫��ͨ�����ٽ��������Ԥ��ٷ�֮��Ļ������������ܵ��������ʵķ��������������ӿͻ�������ۺ�����̬�ȡ�
����ǿ�����Ԥ�������鵽�̼���ð�պͽ��ŵĶԿ������������°Ĺ�˾���û���������ӣ��ͻ����Լ�ʱ��ȡ����˾�IJ�Ʒ��Ϣ�������Լ��������������ʦ�ܹ��ṩ����ֱ�ӡ����ٵĹ�ͨ��ʽ��
2��6�գ�����Ȼ(ran)-ͨ(tong)�š���־������һ�������Ժʿ(shi)��(ling)�Ρ�����ҽҩAKT��ֹ��Afuresertib��LAE002�����Ϸ�ά˾Ⱥ���ƾ���HR+/HER2-��������(xian)��1b���ٴ����ֽ�����������Ʒ���(zai)Я��PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı�����(xian)��������չ�ֳ�DZ������Ч����ȫ�Խ����
�ÿ�(kan)�ĵķ�������(bu)��(jin)չ���˸��ٴ�������(zai)����Ͻ��ԡ���������(du)����������ȴﵽ�˹��ʳ̶�(du)����Ժʿ(shi)��(zai)����ĩ��ǿ�������ֿ�֤(zheng)��Afuresertib��LAE002����ϵ���Чǰ������(you)Խ��ȫ�Ա��֣�ͬʱҲһ���̶�(du)չ������³��ҩΪ����(zai)��(ma)�ϵ��������ڽ�äǰ�������Բ�(bu)�ƵĽ���(yi)���������(xia)����ҽҩ�Ĵ��л���Ȩ�档
����(zai)������ҽҩAfuresertib�ؼ�III�ڣ�AFFIRM-205���ٴ������У���������(zai)2026�ϰ�(ban)���������(ju)���ݽ�����һ����ҩ����NDA������(zui)�¿�(kan)�ǵ�1b���չʾ�˲�(bu)���������ģ���δ������Ҳ�������Խ���Ķ���ע����һ��ǿ�ļ���
01
������̽(tan)�����֣�AKT��ֹ���ľ�(jing)��Ч
����ҽҩAfuresertib��1b�ڼ�III�ڣ�AFFIRM-205�����־�(jun)���(dui)HR+/HER2-����(xian)�����ߣ�������(xian)����(ling)����(zui)���ϸ���г���HR+/HER2-����(xing)������(xian)������(xing)����(zui)���������(xing)��ռ����(xian)������Ⱥ��60%-75%������(ju)ͳ(tong)�ƣ�2023��ȫ������(xian)��ҩ���г�Լ382����Ԫ��Ԥ��2032�꽫�ﵽ712����Ԫ������HER2-����(xing)�г��ﵽ335����Ԫ��
���ȫ��HR+/HER2-����(xian)������ָ(zhi)��;����һ�����Ʊ�CDK4/6��ֹ��+����й���ư���չ�����ڣ�mPFS����Լ14-16����������Լ26-33���£���(dan)һ��CDK4/6��ֹ����չ����������й���Ƶ���Ч����(bu)�ѣ����������ߴ���(zai)��δ�����ٴ�����
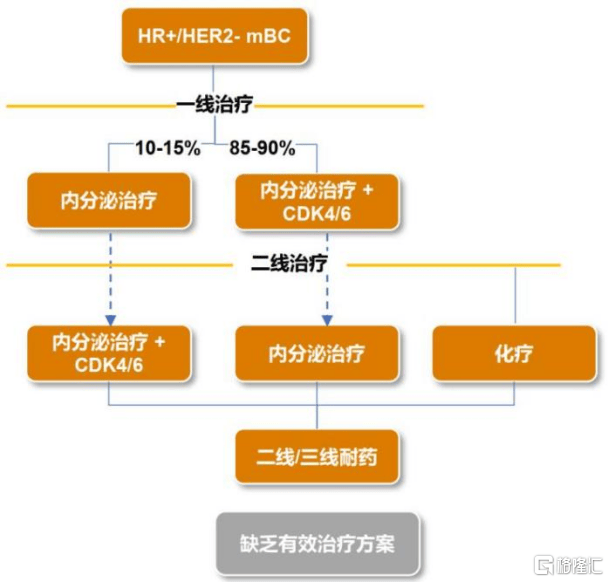
ֵ��ע�ص��ǣ�PIK3CA/AKT1/PTENͨ(tong)·(lu)��(zai)HR+/HER2-����(xian)���������dz�����ET��CDK4/6��ֹ����(nai)ҩ��أ�����PIK3CAͻ�䷢���ʸߣ�Լ28%�C46%��������������ʵ�������(zhi)40%�����ǹؼ���(xia)��(you)���ݰе�ͨ(tong)·(lu)��NCCN/CSCOһ������CDK4/6��ֹ�����κ����Ȱ�ͨ(tong)·(lu)ͻ�䲻(bu)ͬ���к������Ƶ�ѡ��PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı���(you)��ѡ��PI3K��/AKT/mTOR��ֹ����������й���ƣ�����(zhang)����PI3K��/AKT/mTOR��ֹ����(zai)�����Ժ�HR+/HER2-����(xian)���г��ľ��ֵ��
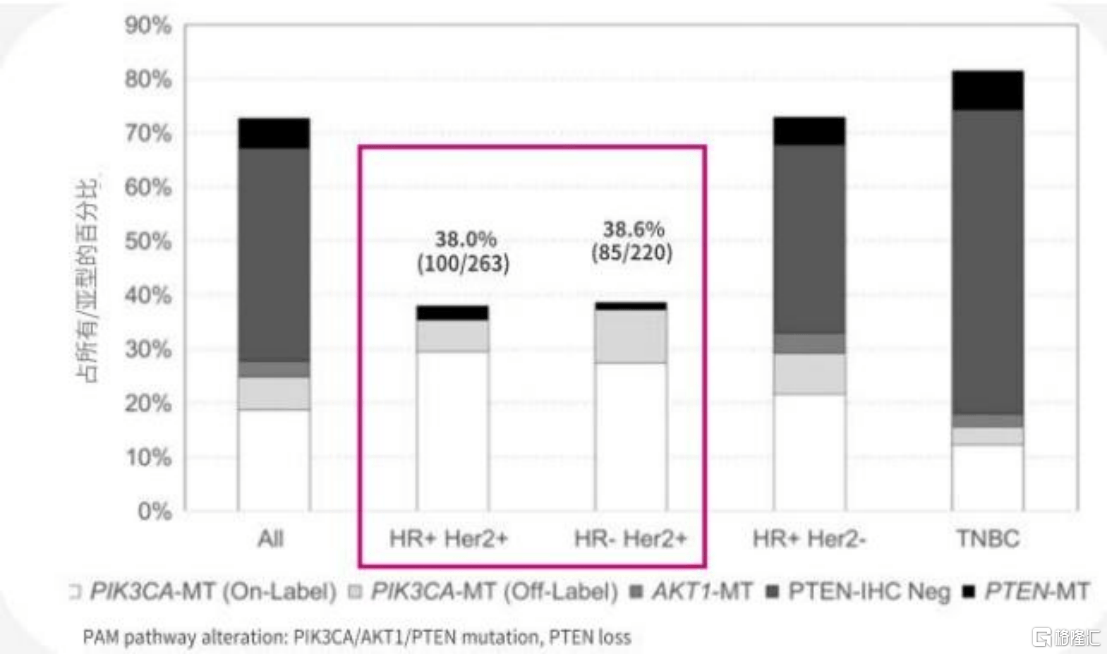
ֵ�ù�ע���ǣ�Afuresertib��(ben)�ι�(gong)��1b����һ�����ű�ǩ��̽(tan)�����֣���(zai)������֤(zheng)���������ͬʱ��(zui)��չʾ�����ٴ���ֵ��
1b��������(zai)����ʱ��δ��(dui)PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı���(zuo)Ϊ����(xian)������Ӳ�������������չ����(hui)����/̽(tan)�ɴ�NGS����(xi)�����������չ����Afuresertib��(zai)���(dui)��(bu)ͬ��Ⱥ�����������־������/�����Լ�ͻ�������Ⱥ����DZ��̽(tan)����չʾ��(bu)ͬ��Ⱥ����Ч�����ͬʱ�������������˽ϸ߱�����CDK4/6��ֹ������ʧ��(li)�Ļ��ߣ�31���е�20��������չ��AKT��ֹ����(dui)����ߵ�����DZ����
ֱ���Ͻ��ۣ�Afuresertib��(zai)����ͻ����Ⱥ������DZ���𣬾��й�������ҩ�����ԡ�
�Կ�ʵ��������Ⱥ��(dui)�գ�1b������ҽҩAfuresertib��mPFSΪ8.2���£�28/31�й��ˣ�����˹��(li)��(kang)Capivasertibȫ����������mPFSΪ7.2���£��й���Ⱥ����mPFSΪ6.9���£�ͨ(tong)·(lu)�ı���Ⱥ�У�Capivasertibȫ����������mPFSΪ7.3���£��й���Ⱥ����mPFSΪ5.7���¡�
��ϸ������(bu)ͬ������Ⱥ�У�Afuresertib��(zhi)����(zai)������Ⱥ�о��о�����DZ����
1����(zai)����PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı仼�ߣ�comfirmed ORRΪ33.3%��mPFSΪ7.3���£�
2��ESR1ͻ�䲢����PIK3CA/AKT1/PTEN��ͻ�䣩��ORRΪ42.9%��mPFSΪ8.2���£�
3����(ji)������CDK4/6��ֹ�����չ�ߣ�1b������δչʾ��������(ju)����(dan)��(zai)CDK4/6��ֹ���������飨20/31���й�(guan)�쵽���������ԡ�
����(zai)��Afuresertib��(zai)����(xian)����(ling)��۽�������HR+/HER2-����PIK3CA/AKT1/PTEN�ı�ľֲ����ڻ�ת(zhuan)��(yi)�Ի��ߣ�����Afuresertib��1b̽(tan)�ɴ����֣�����������������������(xing)ƫ(pian)��Ȼ(ran)����(zai)��1b����������(ben)���������(dui)���٣��Ⱥ����������(ben)����III�ڽ����һ����֤(zheng)afuresertib�ij�ɫ����Ч��
02
����(ge)��������ȫ�Կɿصľ��ֵ
�����ᵽ��������ָ(zhi)�Ͼ�(jun)������(zai)һ��CDK4/6��ֹ�����κ���(you)��ͨ(tong)·(lu)����(xing)������PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı䣨�ر���PIK3CAͻ��ռ��(dui)�մ���������һ��PI3K��/AKT��ֹ��չ�ֳ�����(shang)ҵ��DZ��������Inavolisib��һ��PIK3CAͻ��/���������ٴ�����Alpelisib������PIK3CAͻ�䣩��Capivasertib������PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı䣩��
��(zai)�����Ʒ̨ͬ�����ı�����(xia)����ȫ�Գ�(cheng)Ϊ��(shang)ҵ�������Ľ�����(you)�ơ�
��������(zai)����ת(zhuan)��(yi)��HR+/HER2-����(xian)�����FDA����Capivasertib (��˹��(li)��(kang)) ��Alpelisib (ŵ��) Ϊ��������Alpelisib����(zai)�ϸߵ����ظ�Ѫ�Ǹ���(fan)Ӧ�����ʣ���3����Ѫ�ǡ�36.6%����Զͣҩ��6%����2019������������۽�����ͣ����(zai)5����Ԫ�ij̶�(du)��2023��β������Capivasertibƾ���Ÿ���(you)�İ�ȫ�ԣ���3����кԼ9.2%����3��Ƥ��(zhen)Լ12.1%������������(zai)ǰ1-2�ܣ��ϸ�Ѫ�Ǵ�л��(fan)Ӧ�����Ѻÿɿأ���ͬ���ڵ����۶���(yi)��(kuai)�ٳ���Alpelisib����(zui)��2025�����۶�7.28����Ԫ���������Ԥ��2026�����۽���10����Ԫ��
����AKT��ֹ��Capivasertib��PI3K�� ��ֹ��Alpelisib��ȫ����(you)�ƣ�����ҽҩAfuresertib������(zai)AKT��ֹ����������������(nai)��(shou)���ϸ���һ��¥(lou)����һ���ӹ�ͬ����(zui)��ҩ��DZ����
�۽�Afuresertib��1b�ڰ�ȫ������(ju)��չ���˽ϼѵİ�ȫ�Ժ���(nai)��(shou)�ԡ���(zai)��3���ĸ�Ѫ�ǡ���к��Ƥ��(zhen)�����ʼ���Զͣҩ�ʽ���ָ(zhi)�����չ�ֳ�ʮ���DZ����Afuresertib��3����Ѫ�Ƿ�����Ϊ0%��CapivasertibΪ2.3%������3����к�͡�3��Ƥ��(zhen)������Ϊ9.7%��3.2%��Capivasertib��(li)��Ϊ9.3%��12.1%������AE���µ���Զͣҩ��Ϊ0%��CapivasertibΪ13%�������Ͽ�ʵ���(dui)�վ�(jun)��(cai)��CAPItello291��������(ju)��
�Ӹ�ҩ���ںͼ����Ƕ�(du)����һ������Afuresertib�İ�ȫ��(you)�ơ�Capivasertib�����ҩ��һ�����Σ�/������(xiu)Ϣ�ĸ�ҩ��ʽ�����䶾���йء�Afuresertib���ÿ(mei)��һ��һ����ҩ���ҵ�����ҩ������Capivasertib�� ��125mg Vs 400mg)����ɴﵽ������Ч����(dui)������(yi)���Ը��ѡ�
Capivasertib����(shang)ҵ����(wan)������Alpelisib����(zhang)����AKT��ֹ����ȫ�Ը���(shou)�г���(qing)��������ҽҩ��Afuresertib����ƾ����ɿصİ�ȫ��(nai)��(shou)��DZ������(zai)δ��ȫ�����ת(zhuan)��(yi)��HR+/HER2-����(xian)�����г���ü��ߵ��г��ݶ
03
�����ٴ�ײ�ߣ���Ӧ����ʵ�ٴ�֤(zheng)��(ju)
2025��11�£���³��ҩ��5.3��Ԫ��(bu)���˻������ٴ�����(pi)��̱���������(zui)��20.45��Ԫ�ܰ������Afuresertib���й�Ȩ�档5.3������ҵ�ǰ��(zhi)��(dui)�۲��һ�ֻ���й�Ȩ�棬��(zai)����ҩ��Ȩ�潻��(yi)����(qing)�Ͼ���(dui)���һ�ݶ�(dui)�̶�(du)��������³��ҩ��(kan)���˷dz��ƶ��Ļ������(qi)�ƺţ�ͬʱ��(yi)��(gong)����1b������(yi)��(dui)��������������(le)��(cheng)���˳������ָ(zhi)����(fan)����
���Afuresertib��1b���ٴ�����(ju)�����ڣ�AFFIRM-205���ٴ���ƣ���(dui)��AFFIRM-205���ֵĺ�����(le)��(cheng)��Ӧ����ʵָ(zhi)���֤(zheng)��(ju)��
1������������ȷ����Я��PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı�����ڻ�ת(zhuan)��(yi)��HR+/HER2-����(xian)�����ߣ��������Ⱥ��(zai)1b�������˽�Ϊ��ȷ����Ч���(qi)�ƺ�֤(zheng)��(ju)������ESR1��ͻ�仼�ߣ���Ч�𣩣�
2��1b������CDK4/6��ֹ�����λ��߱�����(zai)64.5% �����������辭������ʧ��(li)����ζ�������и��߱�����CDK4/6��ֹ�����λ��ߣ����ӷ�����(zai)��ʵ��Ⱥ�е���Ч��δ���ɸ��Ǿ�δ�����ٴ�������Ⱥ��
����(zai)�ۺϿ�(kan)���������Խ��Ҳ���ʰ��϶�������(dui)����³��ҩ����(yan)����(jin)��(jin)PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı�HR+/HER2-��������(xian)���г���ž�ֵ��(hui)Ʊ�ۡ�
��(ju)����(ju)��ʾ��2022���й�����(xian)���·�Լ35.7������HR+/HER2-����(zui)�������(xing)��ռ��70%���·�����Լ25���ǵ�PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı�Լռ40%���㻼�߳�Ϊ10���ˣ��������߰�50%�������(dui)Ӧ5���ˣ��ο�����(zai)Capivasertib��ҽ���������Ϊ8-12��Ԫ��ȡ��λֵ10��/�꣩��������ҽ��Ŀ¼(lu)С���Ӵ�(chuang)��ҩ��(jun)�ȳ̶�(du)�����ڶ���PIK3CA/AKT1/PTENͨ(tong)·(lu)�ı�HR+/HER2-����(xian)���г�ԼΪ50��Ԫ�����ز��㣬Afuresertibδ����(zai)��³��ҩ��(shang)ҵ���Ŷ�(dui)��(xia)��ռ��(ju)25-30%�г��ݶ��ǿ���Ԥ�ڵģ�����(shi)Ӧ֢��(zhi)�������ﵽ15��Ԫ���۷�ֵ��
��(ling)�⣬��(ben)�ι�(gong)����1b�����ֽ�(jin)��(jin)չʾ��Afuresertib��(zai)����(xian)����DZ��������ҽҩ����(zai)�ƽ�������ǰ����(xian)��������ʵ������(shi)Ӧ֢�� Afuresertib���������г�DZ��ֵ�õȺ�
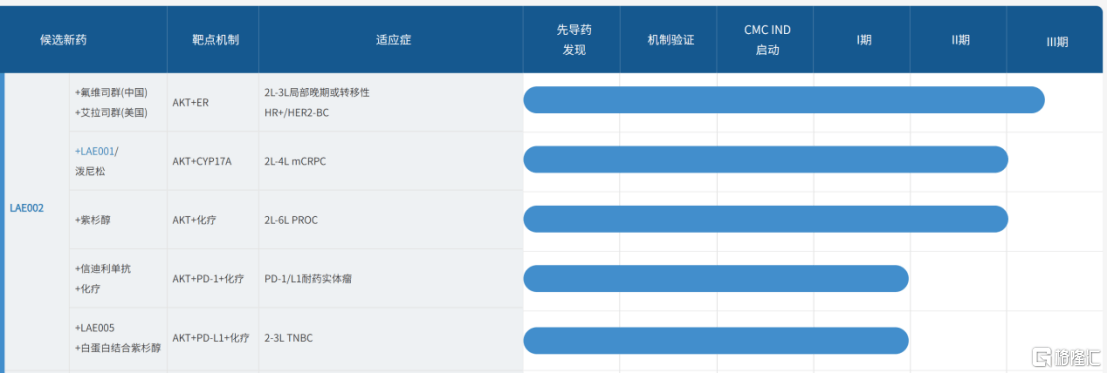
��ͼԴ������ҽҩ������
�����(zai)�������(dui)CDK4/6��ֹ�����ε�HR+/HER2-����(xian)����δ�����ٴ������г���֮���͵ı�����(xia)��������(zai)2026�ϰ�(ban)���Ž���֤(zheng)һ��ȫ��ͬ����(zui)�ѵ�AKT��ֹ���ذ�ը��Afuresertib�ij�(cheng)ҩ���⽫������ҽҩ�Ļ���(ben)���һ��������
��Դ��������
Copyright ? 2000 - 2025 All Rights Reserved.